Simbolo dell’elemento: O
Numero atomico: 8
Config. elettronica: [He] 2s22p4
Isotopi naturali: 16O,17O,18O,
Massa atomica: 16.00 uma
Densita: 1.43 g dm-3 (0°C, 1atm)
Punto di fusione: -219°C
Punto di ebollizione: -183°C
Elettronegativita: 3.50
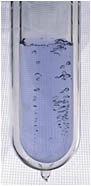
Ossigeno liquido a -183°C
Ossigeno
L' Ossigeno (il nome deriva dal greco «oxys geinomai» cioè generatore di acidi, perché Lavoisier pensava che tutti gli acidi avessero in comune la presenza di questo elemento assieme ad altri non metalli) è un elemento non metallico. Esiste in natura in forma elementare di molecole biatomiche nell’atmosfera, generato nella fotosintesi delle piante. E’ abbondantissimo nella gran parte delle rocce (carbonati e silicati), come componente nell’acqua e nel gas biossido di carbonio. In forma elementare liquida e solida a bassissime temperature è di colore azzurro ed è paramagnetico. Dopo il fluoro è il più elettronegativo e per tale reattività forma composti con quasi tutti gli altri elementi. L'ossigeno trova impiego come ossidante e comburente. Nella forma liquida è usato come ossidante nella propulsione dei razzi. L’ossigeno gassoso è essenziale per la respirazione, e viene utilizzato in medicina in ambito ospedaliero e negli aeroplani come riserva d'aria. L'ossigeno è un blando euforizzante e nel XIX° secolo assieme al protossido d'azoto dava un effetto analgesico. L'ossigeno si lega in modi diversi a seconda dell'elemento e delle condizioni. Può formare ossidi, perossidi, superossidi o idrossidi. L'ossigeno esiste in natura anche sotto forma di ozono, molecole triatomiche, che si forma da scariche elettrostatiche in presenza di ossigeno molecolare e costituisce uno strato nell’alta atmosfera che protegge la superficie terrestre da radiazioni UV altamente ionizzanti.
